
社会の中で企業活動を継続していくためには、コンプライアンスを徹底することが欠かせません。
当社グループでは、グローバルに事業を展開する製薬企業として、コンプライアンスを、私たちを取り巻く「多種多様なステークホルダーの信頼に応え続けていく」ことと捉え、法令及び業界ルールの遵守に留まらず、社内規範はもちろん、社会的良識、理念、社会貢献に配慮した高い倫理観をもって活動することとしています。
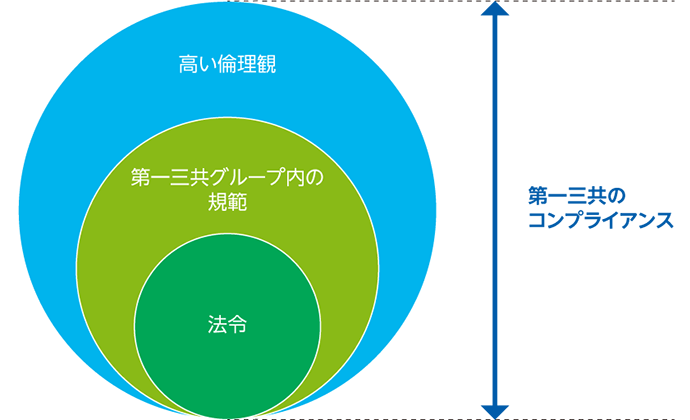
基本的な考え方
当社グループは、コア・バリューの1つに「Integrity」を掲げ、コンプライアンスを意思決定や価値判断の基準とし、グローバルな企業活動において、生命関連企業としてふさわしい高い倫理観をもって行動するコンプライアンス経営を実践しています。
社員がこの考え方について理解を深め、実際に体現できるように、当社グループ共通の行動規範として「第一三共グループ企業行動憲章」及び「第一三共グループ個人行動規範」を定めています。また、これらの精神に基づいた具体的な社内規程として、当社グループはそれぞれの地域における社会的要請に応じたコンプライアンス行動基準等を策定し、役員及び社員に周知徹底しています。
内部統制体制とコンプライアンス
当社グループは、役員及び社員が業務を遂行するにあたり、高い倫理観をもって、法令、業界ルール及び当社グループの行動規範・社内諸規程を遵守すること、並びにこれを担保する内部統制体制を構築することが、継続的な企業価値創造における重要課題と位置付け、コンプライアンス体制の整備等を内部統制体制構築の基本方針に定めています。
- 当社グループ会社では、役員及び社員の行動規範として「第一三共グループ企業行動憲章」、「第一三共グループ個人行動規範」等を定めるとともに、各社においてコンプライアンスに係る会議体を設置しており、さらに当社においては社外専門家を含む会議体を設置しグループ全体のコンプライアンス体制を統制しています。
- 加えて、「第一三共グループグローバルマネジメント規程」に従い当社CEOの命を受けた主要な地域・法人・機能の責任者及び各社における「組織管理規程」に従い社長の命を受けた組織長等が主管業務を掌理し、所属員の監督、管理及び指導を行っています。
- 当社の人事管理、法務・コンプライアンス、リスクマネジメント等の体制整備に係るそれぞれの専門機能が、当社及び国内外のグループ会社の各組織への方針伝達と管理、指導を行い、当社の監査部が、当社グループにおける法令、定款及び社内諸規程の遵守状況について、内部監査を実施しています。